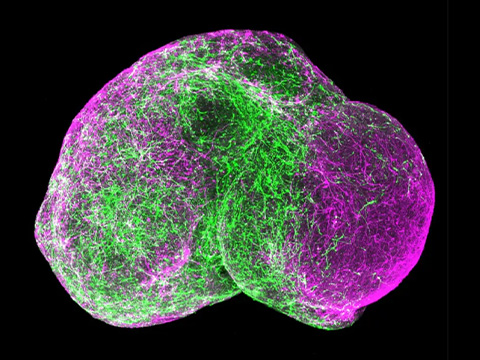
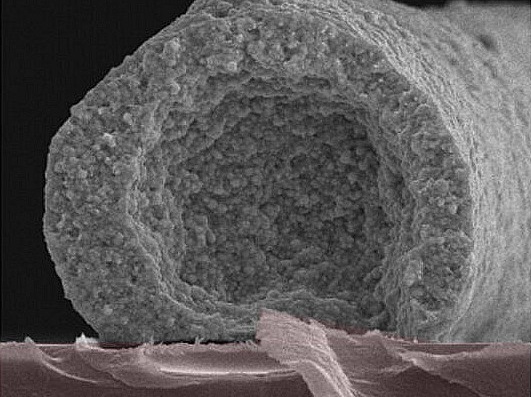
От модели к почти зрелой ткани
Изначально органоиды представляли собой небольшие, размером с горошину, сгустки нейронов, которые позволяли изучать развитие мозга в 3D — в отличие от традиционных двумерных культур клеток. Уже тогда стало ясно, что они необычны: органоиды формировали почти весь набор клеток человеческого мозга, а нейроны демонстрировали спонтанную электрическую активность.
По мере развития технологий исследователи научились:
- формировать в органоидах слоистую структуру, напоминающую кору головного мозга;
- добавлять зачатки сосудистой сети;
- выращивать органоиды, моделирующие разные отделы мозга.
Отдельное направление — создание органоидов из кожных клеток пациентов. Такие модели точно воспроизводят генетические мутации, лежащие в основе нейроразвивающихся расстройств, включая аутизм, и дают возможность тестировать потенциальные методы терапии. В ряде экспериментов пересаженные в мозг грызунов органоиды даже формировали функциональные нейронные связи с тканями хозяина.
Ассемблоиды и «франкенштейновские» сборки
Следующий шаг — так называемые ассемблоиды: конструкции, в которых мозговые органоиды объединяют с другими тканями, например мышцами или кровеносными сосудами. Такие системы позволяют изучать, как мозг управляет функциями организма и что происходит, когда эти связи нарушаются.
Чем больше органоиды начинают напоминать настоящую нервную ткань, тем острее встаёт вопрос: где проходит граница допустимого эксперимента?
Пока — не сознание, но вопросы уже здесь
На сегодняшний день нет доказательств, что мозговые органоиды способны мыслить, осознавать себя или чувствовать боль. Это не «мозг в банке». Однако сами учёные признают: по мере роста сложности нельзя полностью исключать появление примитивных форм ощущений — и важно заранее понимать, как их распознать и что это будет означать с этической точки зрения.
Одним из наиболее тревожных сигналов стало появление долгоживущих органоидов.
Органоиды, которые «стареют»
Команда Паулы Арлотты из Гарварда разработала методы поддержания мозговых органоидов в живом состоянии до семи лет. Каждый такой органоид — меньше горошины — содержит до двух миллионов нейронов и других клеток мозга.
Многолетние наблюдения показали, что органоиды проходят стадии, удивительно похожие на развитие человеческого мозга. В недавнем препринте Арлотта и её коллеги описали, как по мере «старения» меняются:
- нейронная проводка,
- экспрессия генов,
- темпы созревания клеток-предшественников.
Если в молодых органоидах клетки долго «решают», кем стать, то в старых — специализация происходит быстрее. Нейроны пятилетних органоидов по форме, функциям и связям начинают напоминать нейроны ребёнка дошкольного возраста.
Зачем это нужно науке и медицине
Такие модели открывают доступ к ранее недостижимым этапам развития человеческого мозга. Их используют для:
- отслеживания происхождения и миграции разных типов нейронов;
- моделирования аутизма и редких наследственных заболеваний;
- тестирования потенциальных лекарств.
Именно высокая медицинская ценность делает вопрос этики особенно острым.
Где проходит этическая граница
Арлотта и другие ведущие исследователи недавно выступили с призывом создать глобальный орган регулирования, который сопровождал бы развитие этой области — по аналогии с Международным обществом исследований стволовых клеток.
Опасения связаны не только с теоретическим сознанием органоидов. В числе обсуждаемых вопросов:
- могут ли органоиды использоваться в биокомпьютерах и проявлять зачатки интеллекта;
- этично ли имплантировать человеческие мини-мозги животным, если они интегрируются с мозгом хозяина;
- допустима ли пересадка выращенной в лаборатории нейронной ткани человеку.
История биомедицины показывает, что игнорирование этики чревато последствиями — достаточно вспомнить скандал с генетически модифицированными детьми в Китае в 2018 году.
«Путь боли» как предупреждение
На конференции, прошедшей в ноябре при участии исследователей, этиков и представителей пациентских сообществ, особое внимание привлекла работа Серджиу Паски из Стэнфорда. Его команда соединила четыре органоида в нейронный «путь боли», включающий сенсорные нейроны, структуры спинного мозга и коры.
При воздействии химического раздражителя система демонстрировала синхронизированную нейронную активность, указывающую на передачу сигнала. Это не означает, что органоид «чувствовал боль»: для субъективного переживания требуется другой нейронный контур, которого в модели не было. Но эксперимент наглядно показал, насколько близко исследования подходят к функциональным аналогам сенсорных систем.
Между надеждой и осторожностью
Пациенты и их семьи на конференции подчёркивали: органоиды дают реальную надежду на лечение редких и тяжёлых заболеваний. Команда Паски, например, уже получила обнадёживающие результаты при моделировании синдрома Тимоти — редкого генетического расстройства, связанного с аутизмом, эпилепсией и смертельными сердечными нарушениями. Терапия, проверенная на органоидах и грызунах, может в ближайшее время перейти к клиническим испытаниям.
Что дальше
Проведение чёткой границы в исследованиях мозговых органоидов потребует международного сотрудничества. Как отмечают Арлотта, Паска и их коллеги, необходим постоянный глобальный процесс мониторинга и консультирования, который будет развиваться вместе с наукой.
Пока универсальных правил нет, но ясно одно: по мере того как «мини-мозги» становятся всё менее «мини», этика перестаёт быть второстепенным вопросом и становится частью самой технологии.
Источник: https://singularityhub.com/2025/12/25/five-year-old-mini-brains-can-now-mimic-a-kindergarteners-neur...Если вам понравился материал, кликните значок — вы поможете нам узнать, каким статьям и новостям следует отдавать предпочтение. Если вы хотите обсудить материал —не стесняйтесь оставлять свои комментарии : возможно, они будут полезны другим нашим читателям!