Предпосылки и основания изобретения в области нейростимуляции
Нейростимуляция как направление медицинских инвазивных практик довольно распространена в мире для помощи в лечении и облегчении симптомов большого депрессивного расстройства, включая трудно поддающиеся лечению случаи резистентной к терапии депрессии. До недавнего времени пациенты либо лечились амбулаторно, с посещением врача в поликлинике для регулярных сеансов психотерапии и иных рекомендованных медицинских мероприятий: бассейн, прогулки, ароматерапия и др., либо им проводили операции на открытом мозге для имплантации устройства нейростимуляции.Надо вспомнить, что депрессия как аффективное расстройство настроения даже в международной классификации болезней 11-й версии (МКБ-11, внедряемой в России в 4 этапа на протяжении нескольких лет) предполагает более 10 позиций-диагнозов. В практике типично не чисто аффективное расстройство настроения, а смешанное депрессивное и тревожное расстройство, имеющее свою структуру [3, 4]. И есть большой опыт лечения аффективных расстройств настроения, в том числе лечат и бессонницу при депрессии [4].
В прикладном направлении для начала важно определить и классифицировать депрессивное состояние, принять как данность ощущение и состояние, отличное от того, что было раньше. Однако ещё до того, как побороться с недугом или обратиться за помощью к дипломированным специалистам, мудрый человек озаботится превентивными (предварительными) действиями, чтобы бессонницы не случилось. Речь о здоровом образе жизни и прогулках (или пробежках, занятиях плаванием в бассейне – кому как удобно) перед сном. Рекомендуются дыхательные и физические упражнения с незначительным повышением нагрузки – от одного занятия к другому. Компания Motif Neurotech из США с помощью новой электронной технологии изменила эту привычную и известную схему. Результаты исследования, проведённого под контролем учёных в медицинском центре Baylor St. Luke’s (Хьюстон, США), показали, что устройство DOT можно безопасно для человека имплантировать в черепную коробку и воздействовать на сензитивную область мозга для нейростимулирующей терапии. Специалисты медицинских технологий уже окрестили это устройство «мозговым кардиостимулятором». Внешний вид миниатюрного имплантата для лечения депрессии представлен на рис. 1.
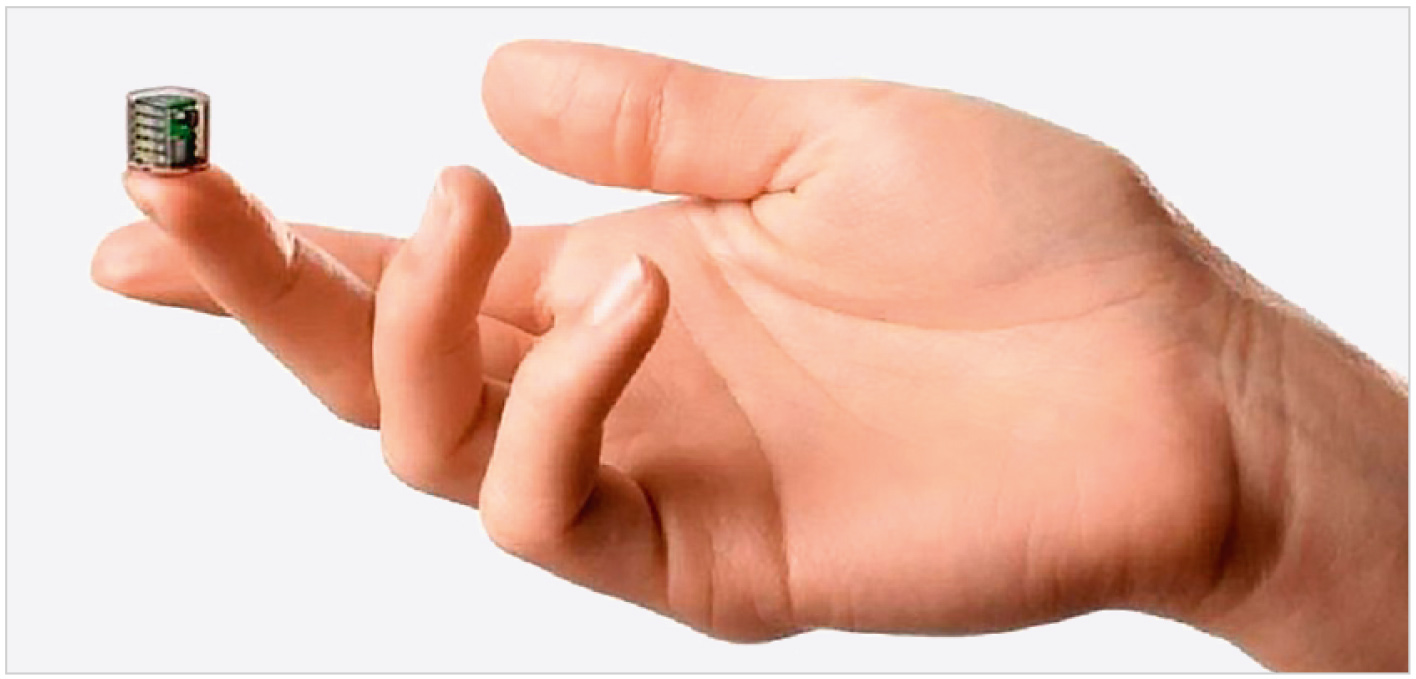
Так, нейромодуляционный имплантат позволяет проводить терапию не выходя из дома и не прибегая к сложным инвазивным и рискованным хирургическим вмешательствам. Исследования проводились более двух лет: сначала на животных, затем с давшими медицинское согласие пациентами – под особым контролем и сопровождением врачей. По сути, речь о большой и перспективной научной работе, в которой участвуют высококлассные специалисты, уже имеющие в своём бэкграунде запатентованные разработки в области медицинской РЭА. По первым апробированным результатам, разумеется, некорректно говорить о надёжности и долгосрочной перспективе сего электронного устройства, однако примем во внимание, что в медицинской области почти все лекарственные препараты, и тем более медтехника, «выдерживают» длительные испытания и апробацию на реферативных группах пациентов, прежде чем бывают рекомендованы к массовому применению. В данном случае мы говорим о перспективной разработке, и, конечно же, её будут совершенствовать. Но идея уже имеет реализованный образец, модель, получившую подтверждение в безопасности использования и результативности терапии при минимально инвазивном подходе к использованию нейростимуляции для лечения тяжелой депрессии. Первый ультрамалых размеров бессвинцовый стимулятор мозга у человека – это цифровой программируемый надмозговой терапевтический прибор (или DOT), способный генерировать достаточно энергии для стимуляции мозговой активности человека и крупных животных через твёрдую мозговую оболочку. DOT реализован в стеклянном корпусе и обеспечивает надёжную работу и не сковывает движения пациента, может работать без переустановки до 1 месяца. Поэтому устройство столь перспективно и подходит для использования в домашних условиях для терапевтического лечения различных психических расстройств.
Особенности устройства и его установки
Модель производства компании Motif Neurotech позиционируется как электронное устройство (Digitally Programmable Over-Brain Therapeutic – DOT) и является цифровым программируемым терапевтическим прибором с фиксацией непосредственно над головным мозгом. Финансирование работы предоставлено Фондом Макнейра. Среди учёных и исследователей-разработчиков Joshua E. Woods, Amanda L. Singer, Fatima Alrashdan, Wendy Tan, Chunfeng Tan, Sunil A. Sheth, Sameer A. Sheth, Jacob T. Robinson (все из США). Cертифицирующий орган IRB предоставил одобрение устройства после его испытания в медицинском колледже Бейлора. Таким образом, устройство способно стабильно обеспечивать безопасную и эффективную стимуляцию мозга, что подтверждено испытаниями [5].Устройство имеет малый размер и площадь не более 1 см² в поперечном сечении. Не имеет источника питания и связано с внешним контроллером, а также облачным хранилищем данных беспроводным способом по каналу Wi-Fi. Реализованная в корпусе устройства отдельная магнитная катушка и система драйверов для обеспечения беспроводной связи обеспечивают питание непосредственно на имплантат, размещённый в стеклянном корпусе, где находится и электрод для стимуляции. Корпус устройства с расположением элементов представлен на рис. 2.

Тем же каналом беспроводной связи обеспечивается обмен данных в цифровом формате. К электронному устройству разработана гарнитура для удобства и регулярных сеансов работы. Миниатюрное DOT-беспроводное устройство не соприкасается с мозгом или его защитной оболочкой. Устанавливается в 14-мм отверстие в черепной коробке в ходе малоинвазивной, гигиеничной и условно безопасной амбулаторной процедуры продолжительностью всего 20 минут [1].
Принцип работы устройства
Рефрактерные неврологические и психические расстройства всё чаще лечат с помощью методов стимуляции мозга с использованием имплантированных устройств: способом нейромодуляции. Однако существующие коммерчески доступные системы электронно-медицинского оборудования ограничены и нуждаются в имплантируемых генераторах импульсов и электропитании с помощью проводов. Условная сложность сей архитектуры создаёт множество критичных вопросов, требующих решения медицинскими и технологическими методами. Так, в проблемном поле частицы инородных материалов, к примеру, свинца, которые угрожают пациенту инфекцией и осложнениями недуга. Именно поэтому внедрение неинвазивных подходов расширило доступ и к инновационным методам лечения. Обсуждая модель компании Motif, имеем в виду бессвинцовый нейростимулятор. Такое медицинское устройство вырабатывает достаточное количество энергии для стимуляции активности коры головного мозга под стимулирующим воздействием через твёрдую мозговую оболочку. Экстремальная система воздействия возможна с помощью беспроводной передачи сигналов слабого тока магнитоэлектрическим способом, но без прямого контакта с кортикальной областью мозга. Внешняя стимуляция коры головного мозга (XCS) открывает возможность проведения условно простых малоинвазивных хирургических процедур, обеспечивающих точную, длительную нейромодуляцию в домашних условиях с помощью крошечных имплантатов, которые никогда прямо не соприкасаются с поверхностью мозга.Особенности транскраниальной магнитной стимуляции
Когда фармацевтические препараты неэффективны или вызывают невыносимые побочные эффекты, пациенты и врачи обращаются к нейромодуляции для получения эффективных методов лечения. Так, при болезни Паркинсона (БП) и эссенциального тремора (ЭТ) глубокая стимуляция мозга результативна в лечении тремора и других симптомов. При тяжёлом депрессивном расстройстве (МДД) и обсессивно-компульсивном расстройстве (ОКР) нейрофизиологическое модулирование активности в определённых областях мозга обеспечивает эффективную терапию, когда лекарственные препараты не обеспечивают адекватного лечения. В данном случае транскраниальная магнитная стимуляция (ТМС, TMS) является показательным примером метода применения нейромозговой стимуляции. ТМС может неинвазивно активировать небольшие участки поверхности мозга размером от нескольких миллиметров до нескольких сантиметров, используя генерируемое извне магнитное поле мощностью 1–2 Т (Тесла), и дать хороший результат выздоровления пациента при лечении нервно-психических расстройств [2].С 1998 года число клинических испытаний, в которых используется ТМС для лечения нервно-психических расстройств, выросло примерно в 2 раза. Основываясь на данных клинических испытаний, орган сертификации и лицензирования в области медицинских технологий в США (FDA) одобрил TMС для лечения резистентной депрессии, и с тех пор большинство страховых компаний возмещают стоимость мультисессионной терапии в клинике, если пациенты не проходят традиционную терапию антидепрессантами. TMС уже тогда использовали для лечения обсессивно-компульсивного расстройства, ПТСР (посттравматического стрессового расстройства) и болезни Альцгеймера. Хотя ТМС является клинически доказанной терапией, у неё есть ограничения. Во-первых, системы TMС в 2024 году требуют условно больших пиковых мощностей до 3 МВт, а это означает, что пока они одобрены только для использования в стационаре. В результате TMС недоступна для пациентов, живущих удалённо. Во-вторых, от сеанса к сеансу таргетинг может быть разным, поскольку стимулятор необходимо настраивать каждый раз перед процедурой с конкретным пациентом. Да, существуют условно альтернативные неинвазивные способы стимуляции мозга, как транскраниальная стимуляция постоянным током (TDCS) и транскраниальная стимуляция переменным током (TACS). Однако технологию стимуляции нервной системы в домашних условиях широко не использовали, потому что электрическое поле, создаваемое неинвазивным электростимулятором, не могло достигать напряжённости поля, необходимого для непосредственного воздействия [6]. При этом задача стояла активировать область мозга, не активируя при этом нервы в волосистой части головы, которые вызывают болезненные побочные эффекты. В сравнении со всеми названными методами и технологиями имплантируемые стимуляторы могут обеспечивать точную электрическую стимуляцию, которая непрерывно активирует мозг, но и эти имплантаты требовали сложной хирургической процедуры – и это также являлось ограничением для большого числа пациентов. По технологии беспроводной передачи энергии (WPT) создан кортикальный стимулятор мозга с достаточной энергией и устойчивостью (надёжностью работы) как аналог TMС. Минимально инвазивные процедуры не предполагают контакта с мозгом или перфорации защитной твёрдой мозговой оболочки, а концепция терапии «кортикальной стимуляции с внешним питанием» (XCS) оказалась ещё более эффективной, чем TMС, и такой же точной и удобной, как традиционные имплантируемые стимуляторы со встроенными и перезаряжаемыми элементами питания.
Электронный стимулятор состоит из имплантируемого генератора импульсов (IPG), работающего на встроенных элементах питания – батарейках и подключаемого проводами к участку стимуляции. К примеру, когда IPG имплантируются в грудную клетку, электрические провода проходят вблизи головы и шеи, а частые движения приводят к смещению имплантата и в целом его малой эффективности.
В альтернативе уместно имплантировать IPG в черепную коробку, но это невозможно без трепанации черепа пациента. Тем не менее и такие электронные приборы – условные анахронизмы эпохи – с разной результативностью, но используются для лечения аффективных расстройств настроения, доказывая, что долговременный эффект облегчения психических расстройств возможен при прямой электрической стимуляции с помощью имплантатов. Электроды, размещённые над дорсолатеральной префронтальной корой (DLPFC) – участка, «одобренного» для воздействия устройствами медицинской электроники FDA для ТМС-терапии, в исследовании показали антидепрессивный эффект у 3 из 5 пациентов [6]. Глубокая стимуляция мозга (DBS) нескольких участков внутри коры головного мозга также дала результат и антидепрессивные эффекты с облегчением от ОКР. Нейромодуляция может быть достигнута без IPG: с помощью подкожных проводников, подключающихся к внешнему стимулятору; однако возможная (нестерильная) инфекция от внешних устройств и применение условно тонких электрических проводников накладывают ограничения на образ жизни (комфортное состояние) пациента в процессе медицинского воздействия и типично не используются для длительной терапии нейромодуляцией.
Несмотря на растущую популярность беспроводных технологий в устройствах стимуляции без использования внутренних источников питания, клинические системы нейромодуляции до 2023 года применялись только в периферической нервной системе, не имея компактного миниатюрного форм-фактора, чтобы их можно было быстро, гигиенично и безопасно «встроить» в черепную коробку. Доклинические исследования на грызунах показали результативность стимуляции коры головного мозга, но показали и другое: амплитуда импульсного воздействия слишком мала, чтобы стимулировать человеческий мозг воздействием через условно твёрдую мозговую оболочку. Единственный известный в научных кругах эпидуральный кортикальный стимулятор без батареек был применён на кошке, но её приходилось обездвиживать (что вызывало дополнительные стрессовые факторы у животного, притом что наркоз в таком воздействии не имел смысла). И движение животного, смещение стимулятора всего на 3 мм существенно затрудняли достижение эффективного результата терапии как в условиях операционной, так и дома.
Основной проблемой при создании DOT является обеспечение достаточной мощности для стимуляции мозга из эпидурального пространства. Источник питания или батарея является самым объёмным компонентом имплантируемого нейронного стимулятора. А в рассматриваемом DOT-устройстве применена технология, позволяющая безопасно подавать беспроводным способом достаточное электропитание с напряжением 10–15 В, необходимым для эпидуральной стимуляции мозга при импедансе примерно 1 кОм. Это значение сопоставимо с условиями результативной стимуляции спинного мозга, но примерно в 5 раз превышает амплитуду стимуляции, необходимую для стимуляции блуждающего нерва (VNS), и в 3 раза превышает амплитуду стимуляции, необходимую для глубокой стимуляции головного мозга (DBS) [5].
Промежуточные результаты
Недавняя разработка магнитоэлектрического беспроводного источника питания теперь позволяет достичь требуемого уровня стимуляции с импульсным модулированным напряжением 14,5 В в имплантатах миллиметрового размера, не требующих использования батареек. Авторы исследования также утверждают, что получили мощность WPT до 56 мВт с использованием магнитоэлектрических плёнок с напряжением до 10 В DC. Чтобы эффективно использовать эту энергию и обеспечить соответствие напряжению 14,5 В на электродах с импедансом 1 кОм, внедрили схему стимуляции, представленную на рис. 3. Здесь представлена интраоперационная демонстрация эпидуральной стимуляции коры головного мозга с помощью миниатюрного эпидурально-кортикального стимулятора-имплантата без встроенных элементов питания.В качестве модулей присутствует адаптер-стабилизатор питания, микроконтроллер с крайне малым энергопотреблением, мультиплексор и усилитель линии связи, а также повышающий преобразователь с выходным напряжением 15 В DC. В специальный стеклянный корпус поместили электроды (один – стимулирующий, используется как передатчик), состоящие из напылённого на поверхность стержня оксида иридия. И такое электронное устройство имеет размеры 9×9×11 мм.
Применительно к рис. 3 [5].
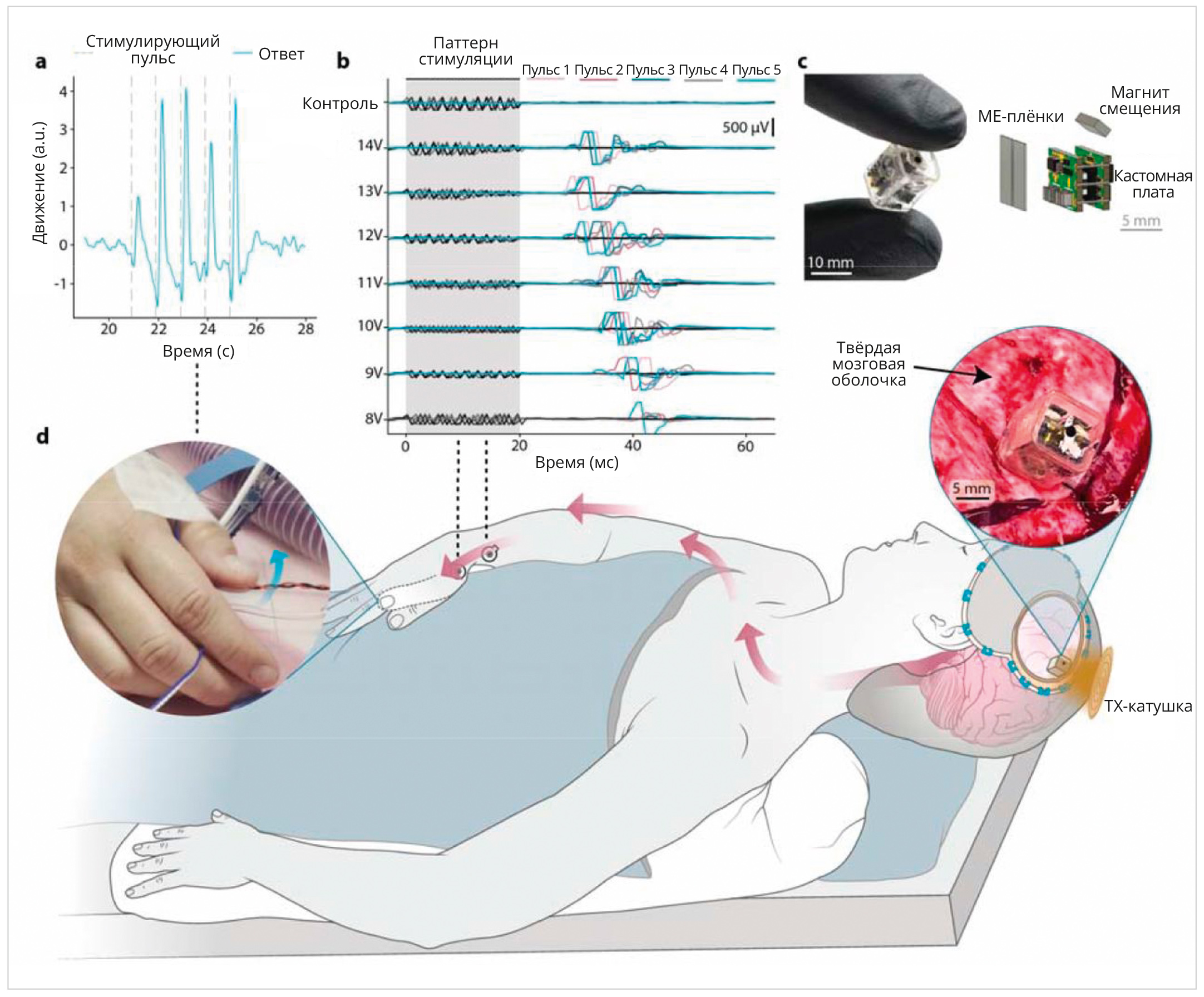
А: Применяется стимулирующее воздействие с частотой 500 Гц в пачке по 10 импульсов и импульсное воздействие с частотой 1 Гц двухфазной амплитудой 12 В.
B: форма ЭМГ (пачки по 5 импульсов) в каждой группе мышц APB-ADM во время стимуляции с различной амплитудой показывают, что эпидуральная стимуляция коры головного мозга вызывает ответный импульс амплитудой около 8 В, то есть примерно 2/3 импульсов воздействуют на нервные окончания.
С: прототип электронного устройства между двумя пальцами руки в перчатке. Показаны внутренние компоненты DOT, состоящие из 2 плёнок ME, панелей печатной платы (PCB), соединённых проводами, и смещающегося магнита.
D: иллюстрация интраоперационных исследований на людях; устройство над твёрдой мозговой оболочкой коры активировано с помощью передатчика импульсов. Фактически моторные реакции человека были таковы, что стимуляция приводила к контралатеральному движению большого пальца. Справа показана иллюстрация зафиксированного над твёрдой мозговой оболочкой устройства.
Для питания и связи с DOT-устройством применили магнитную катушку и передающий микромодуль имплантата. Поток цифровых данных, генерируемый формирователем магнитного поля, программирует имплантат на один из 32 возможных уровней амплитуды стимуляции в диапазоне 6,75–14,5 В, а также устанавливает длительность импульса стимуляции и тип (частоту пачек) импульса (режим) стимуляции. Интраоперационное тестирование во время нейрохирургической процедуры показало, что устройство может стимулировать двигательную реакцию при размещении непосредственно на внешней стороне коры головного мозга, а именно вызвать сокращение кисти человека. В конкретном исследовании пациент проходил процедуру резекции опухоли, которая требовала трепанации черепа, чтобы обнажить кору головного мозга. Запрограммировав DOT в режиме генерации сигнала воздействия: 500 Гц, 10 импульсов с частотой повторения 1 Гц и двухфазной амплитудой 14,5 В, исследователи проанализировали видеозапись сокращения кисти с частотой 1 Гц, подтверждающую, что таким воздействием принудительно (специально) удалось активировать область мозга. Таким же образом по аналогии удавалось вызвать сокращения мышц на пальцах, ладонях, верхних и нижних конечностях человека [5].
Другое проведённое тем же составом исследователей интраоперационное исследование показало, что DOT-устройство может стимулировать аналогичные двигательные реакции при размещении над твёрдой мозговой оболочкой. Отсюда был предложен вывод: несмотря на небольшой форм-фактор имплантата миллиметрового размера, он способен задействовать область коры головного мозга человека примерно с тем же результатом (терапевтическим эффектом), что и процедура ТМС. Электромиографические (ЭМГ) реакции в группах мышц APB-ADM (отводящий Pollicis Brevis, отводящий Digiti Minimi) регистрировались при амплитудах всего 8 В, по мере увеличения интенсивности стимуляции латентность между стимуляцией и отражающим сигналом уменьшалась, а количество вызываемых движений увеличивалось (рис. 3а). Такая локализация реакции на стимуляцию демонстрирует высокую точность определения области активации устройства. Это показывает, что уровень напряжения стимуляции безопасен и достаточен для активации ткани в коре головного мозга человека при фиксации устройства над твёрдой мозговой оболочкой даже сквозь толщу промежуточной ткани.
Организация канала двунаправленной передачи данных
В дополнение к получению беспроводного питания и данных разработчики испытали DOT для передачи сигналов обратно на внешний приёмопередатчик, чтобы записать (зафиксировать в электронной памяти ПК) диагностические свойства имплантата и дистанционно включать технологические функции, такие как запись физиологических сигналов пациента. Чтобы свести к минимуму размер, сложность (интегрированность компонентов) и энергопотребление имплантата, применён эластичный материал ME. Притом каждое сообщение длительностью 3,4 мс разделено мультиплексорами в двух каналах: на 3 бита и, соответственно, 8 бит. Параметры стимуляции задают по первому каналу связи, а обмен данными и измерения проводят по второму. Так, в условной сети передачи данных удалось настроить и обеспечить синхронизацию с помощью внешнего приёмопередатчика. DOT-устройство разработано таким образом, чтобы его выходные данные стимуляции передавались кодом в заключительной части потока данных. Поэтому можно посылать команды на генерации в имплантате желаемой частоты, а двухфазные импульсы или последовательности импульсов вполне могут запускаться с частотой до 250 Гц. Для частот > 250 Гц, к примеру, для стимуляции частотой 500 Гц, выбирают соответствующий режим (последовательности импульсов) во встроенном ПО устройства и запускают функцию с помощью внешнего приёмопередатчика. На рис. 4 представлен метод цифровой двунаправленной связи и эксплуатационные характеристики DOT.Пояснение к рис. 4.
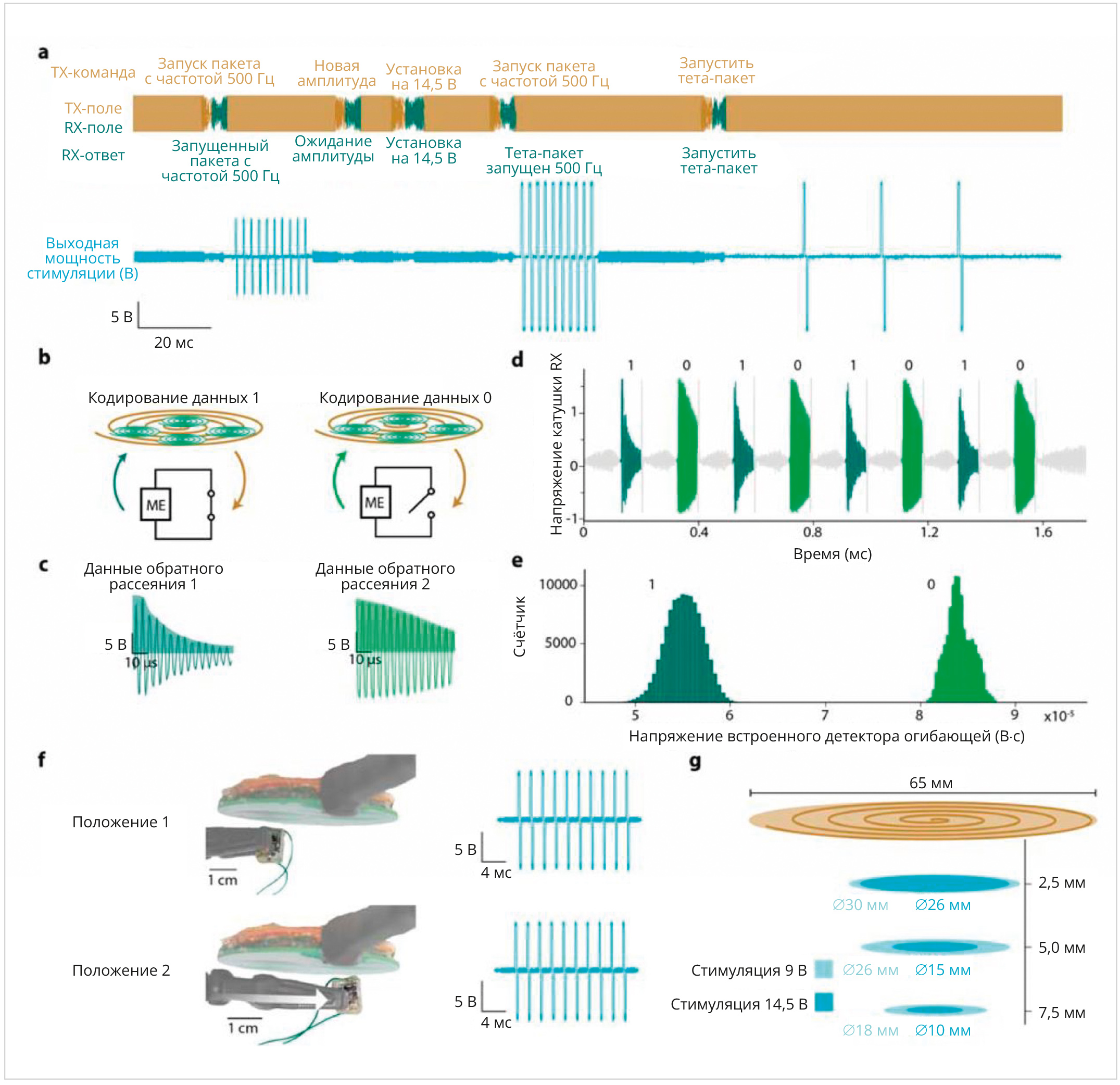
4a: время при генерации импульсов стимуляции в диапазоне ±6,75…±14,5 В с шагом 250 мВ. Пример экспериментальной последовательности выходных сигналов приёмопередатчика и стимуляции имплантата. Приёмопередатчик запускается последовательностями импульсов длительностью 3,4 мс. Устройство было запрограммировано таким образом, чтобы на стимулирующий электрод воздействовали импульсы с частотой 500 Гц пачками по 10.
Для получения диагностической информации от имплантата в режиме реального времени внедрена двухканальная передача данных: для управления (вкл/выкл, активации) магнитным полем обратного рассеяния; и этот режим потребляет крайне мало энергии. Так, передатчик сигналов активируется для возбуждения режима резонанса пленки ME, а затем передатчик деактивируется, но остаточное магнитное поле, генерируемое при затухании резонанса ME, всё ещё обеспечивает питание имплантата. Внутренний переключатель режима работы имплантата модулирует амплитуду отражённого сигнала (рис. 4b).
4b: иллюстрация, показывающая, как цифровые данные кодируются с помощью пассивного обратного рассеяния ME.
Если выход плёнки ME активирован в режиме стимуляции, фронт импульсов будет более длинным, чем без активации МЕ (рис. 4d).
Способ кодирования битов с имплантата. Биты 1 и 0 кодируются путём переключения между короткими (данные 1) и длинными (данные 0) последовательностями. Результирующие биты 0 и 1 разделяются на стороне приёмопередатчика с помощью аналоговой схемы (рис. 4d, e). Магнитоэлектрическая плёнка МЕ, входящая в состав имплантата, возбуждается магнитным полем приёмопередатчика, и тогда поле обратного (отражённого) сигнала измеряется с помощью дифференциально спаренных катушек датчика, в то время как поле возбуждения неактивно. Условная перегрузка на плёнке ME не превышает 40 мс. Цифровые данные из последовательности импульсов декодируются по положительному фронту сигнала.
4d: последовательность 1 и 0 битов, используемая для калибровки порогового значения для различения двух битов, используется в режиме изменений имплантата.
4e: гистограмма, показывающая интегральное напряжение отражённого сигнала «отбоя» для битов 1 и 0 с дискредитацией 223 888 битами при расположении имплантата на расстоянии 1 см от катушек внешнего приёмопередатчика. Биты 1 и 0 разделены, их легко отличить от сигнала приёмника.
4f: два положения, в которых устройство способно выдавать двухфазные последовательности импульсов напряжением 9 В, последовательности из 10 импульсов частотой 500 Гц с напряжённостью поля 7 мТл на поверхности катушки для формирования соответствующего выходного сигнала стимуляции. Расстояние между двумя электродами > 2,5 см, что свидетельствует об относительно большом допуске на смещение устройства в случае возникновения двигательной активности пациента, что в принципе важно в условиях операционной.
4g: график экспериментальных результатов двухфазных последовательных импульсов напряжением 9…14,5 В, пачек по 10 импульсов частотой 500 Гц на разном расстоянии от катушек приёмопередатчика с напряжённостью поля 7 мТл на поверхности катушки. На расстоянии 7,5 мм устройство способно выдавать серии импульсов напряжением 14,5 В при площади воздействия 1 см² и серии импульсов напряжением 9 В при площади 1,8 см².
Беспроводная передача данных обеспечивает надёжную связь с имплантатом в условно неконтролируемых средах, таких как медицинская операционная. Эластичный материал плёнок МЕ обеспечивает устойчивость к их возможному перекосу и деформации при настройке устройства на возбуждение магнитного поля мощностью 7 мТл (в пределах допустимых значений) на поверхности катушки. При генерации импульсов двухфазной стимуляции напряжением 9 В устройство надёжно работало на участке площадью 1,8–2,5 см² в центре катушки приёмопередатчика на расстоянии 7,5 мм от катушки (измерение по центру верхней части устройства). При генерации импульсов двухфазной стимуляции с максимальной амплитудой 14,5 В устройство надёжно работало на площади 0,78 см² на расстоянии 7,5 мм от поверхности катушки (рис. 4g). Такой результат принято считать хорошим в части обеспечения глубины имплантации, основанной на известной средней толщине костей свода черепа взрослого человека в 5,8 мм [5].
О надёжности и безопасности
Работа генератора импульсов оказалась достаточно мощной, чтобы стимулировать кору головного мозга через твёрдую мозговую оболочку, но важны также аспекты обеспечения безопасности использования имплантата. Разработчики подтверждают, что устройство сможет безопасно обеспечить такой же уровень стимуляции с течением времени, если будет имплантировано постоянно. Чтобы доказать этот параметр предметно, использовали в качестве модели свинью, и выбор обоснован тем, что анатомическая структура мозга свиньи и толщина твёрдой мозговой оболочки наиболее соответствуют анатомии тех же частей у человека.В следующем эксперименте протестировали способность DOT-устройства стимулировать неповреждённую твёрдую мозговую оболочку и изучали реакцию тканей на протяжении времени от нескольких часов до 30 суток. Вот как описывают процедуру внедрения имплантата практикующие специалисты. «Операция по имплантации заняла около 20 минут и не предполагала контакта с головным мозгом. Мы обнажили череп и просверлили отверстие диаметром 14 мм над корой головного мозга, обнажив твёрдую мозговую оболочку под ней. Затем мы внедрили имплантат с помощью защитной силиконовой прокладки, поместили в отверстие и закрепили пластиковой крышкой (PEEK) для защиты имплантата от внешних повреждений. Схема полностью имплантированной системы и протокол тестирования показаны на рис. 5». Практика эпидуральной стимуляции коры головного мозга на примере животного вида КРС (крупного рогатого скота) показала, что DOT эффективно восстанавливает активность коры головного мозга в течение 30 дней. На рис. 5 представлена иллюстрация внедрения имплантата в кору мозга животного вида КРС.
На рис. 5 для иллюстрирования предложена схема тестирования устройства во время хронической имплантации на модели свиньи. Стимуляция проводилась над левой моторной корой головного мозга, а изменение под воздействием стимулятора фиксировалось по правой передней конечности свина. Катушка приёмопередатчика фиксировалась над местом имплантации, пока свин был спокоен и расслаблен, а устройство питалось и программировалось с помощью внешнего передатчика. На левой вставке рис. 5 вверху показано поперечное сечение имплантата над твёрдой мозговой оболочкой и под кожей свиньи. На правой вставке (рис. 5 вверху) показан пример оценки движения передних конечностей.
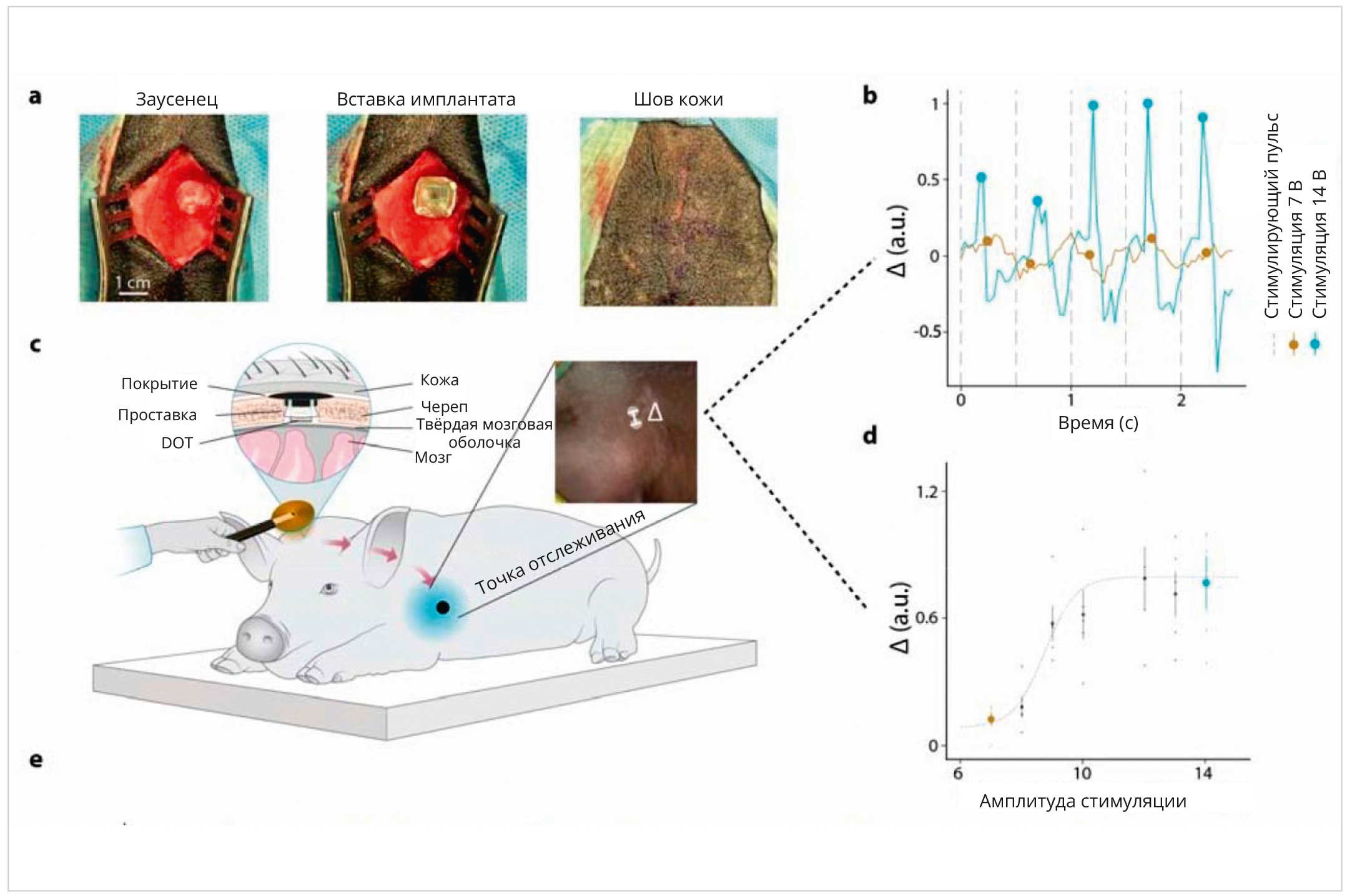
5d: среднее значение на пиках сигнала при увеличении амплитуды стимуляции в диапазоне 7–14 В. Пунктирная линия показывает сигмоидальную подгонку с приблизительным пороговым напряжением воздействия 10 В. Реакция 7 В (жёлтая точка) значительно ниже порога минимального уровня, а реакция 14 В (синяя точка) показывает более высокое смещение, что указывает на движение свиньи в ответ на стимуляцию.
5e вверху: среднее значение амплитуды пиков сигнала за весь период воздействия имплантата. Синие точки показывают среднюю амплитуду после воздействия 5 импульсов напряжением 14 В, а оранжевые точки показывают среднюю амплитуду при стимуляции напряжением 7 В. Во всё время тестирования наблюдался значительно больший отклик при стимуляции напряжением 14 В по сравнению со стимуляцией напряжением 7 В, что свидетельствует о том, что DOT-устройство оставалось функциональным и эффективным при рекрутировании коры мозга в течение всего периода имплантации в 30 дней (t-тест независимых выборок, р < 0,05) [5]. При имплантации устройства на 20–35 дней свиньям над твёрдой мозговой оболочкой устройство вызывало двигательную стимуляцию разной активности. Для «чистоты» и валидности эксперимента исследователи использовали фиктивный имплантат у некоторых животных, чтобы сравнить итоговые результаты и исключить эффект плацебо. Реакции при стимуляции, их продолжительность, направленность и амплитуда фиксировались с помощью инструментов видеоанализа. Между 15-м и 25-м днями наблюдалось увеличение сопротивления электрода, аналогичное тому, которое наблюдалось при импедансе DBS.
В промежутке между этими днями участники исследования отметили уменьшение амплитуды движений при максимальных значениях стимуляции, что коррелировало с увеличением сопротивления. Через 25 дней сопротивление стабилизировалось примерно на уровне 2,25 кОм, что обоснованно связывают с анатомическими изменениями тканей у животного, включая утолщение твёрдой мозговой оболочки или повторный рост тканей в месте приложения имплантата [5]. Эти известные в медицинской практике реакции на инородное тело могут возникать при адаптации субдуральных и эпидуральных имплантатов, но не представляют угрозы безопасности животному или человеку. Поскольку DOT-устройство стабильно обеспечивало стимуляцию мозга, несмотря на увеличение импеданса, это подтверждает его эффективность в нейротерапии даже при наличии реакций организма на инородное тело.
При внимательном анализе дозы терапевтической стимуляции, которую можно получить при ТМС-подобной терапии, не обнаружили критичных или заслуживающих внимания изменений и патологий в стимулируемых областях мозга; это позволяет предположить, что точечная стимуляция может обеспечить безопасный аналог ТМС-терапии. Для этих исследований выбрали способ прерывистой тета-импульсной стимуляции (iTBS), используемый в TMС для стимуляции областей коры импульсами в течение 3 минут. Сигнал состоит из пакетов по 3 импульса частотой 50 Гц, повторяющихся с частотой 5 Гц, то есть с интервалом в 10 с. Исследования показали, что процессы стимуляции, повторяемые 5 дней в неделю в течение 6 недель, обеспечивают эффективную терапию для пациентов с устойчивой к лечению депрессией. Общая доза, получаемая при такой терапии, составляет в общем 60–450 минут стимуляции и соответственно 12 000–90 000 импульсов воздействия. При тестировании безопасности точечной стимуляции применяли «прямую электрическую стимуляцию» iTBS-подобной формы волны двухфазными импульсами по 250 мкс на фазу в течение 300 минут (54 300 импульсов) [6]. У разных животных воздействовали имплантатом в общем 170 и 200 минут iTBS-подобной стимуляцией. Затем исследователи эксплантировали DOT-устройства и вывели животных «на отдых» в течение 7–10 дней, прежде чем их забили для анализа головного мозга и твёрдой мозговой оболочки. Отчёты патологоанатомов после эксплантации не показали различий между мозгом животного без воздействия и стимулирования и твёрдой мозговой оболочкой под стимулятором по сравнению с фиктивным имплантатом того же размера и формы, имплантированным тому же животному на противоположной стороне мозга. У некоторых животных обнаружили незначительные воспалительные реакции как на активные, так и на фиктивные имплантаты, что указывает на вариабельность реакций на инородное тело от животного к животному, но даже в случае реакции на инородное тело DOT-устройство всё ещё может генерировать эффективную стимуляцию коры мозга живого организма, а учёные предполагают, что такая реакция не ограничит способности и медикаментозный эффект нейромодуляционной терапии.
Выводы
Инновационные решения с помощью новых технологий и современной микроэлектроники в традиционной архитектуре нейромодуляции приведут к появлению новых парадигм клинической терапии. К примеру, эпизодическая нейромодуляция эффективна при ТМС и может безопасно применяться в домашних условиях с помощью миниатюрного имплантата в сочетании с носимой гарнитурой.Так сокращается время на обслуживание пациентов в стационаре и организационные затраты на обучение специально-обучаемого персонала, обеспечение койко-мест в больницах и медицинского сопровождения пациентов. Условная простота, безопасность внедрения (применения) и минимальное время настройки (подготовки) имплантата, в котором отсутствует автономный элемент питания, даёт устройству ещё больше конкурентных возможностей и автономности. Кроме того, концепция функционирования XCS может быть расширена, чтобы стимулировать несколько областей мозга для управления определёнными паттернами активности или состояниями пациента. Так, двустороннее воздействие терапией с помощью имплантата над левой и правой дорсолатеральной префронтальной корой привело к медицински результативной терапии для пациентов с суицидальными мыслями.
Отсутствие проводов или батареек значительно упрощает операцию и устраняет критические опасности, однако остаются актуальными инженерные задачи, связанные с внедрением даже этой апробированной концепции DOT в имплантат для постоянного использования человеком. Производство и испытания продолжаются в соответствии с нормативными стандартами, необходимыми для получения одобрения (сертификации) FDA, включая тестирование долгосрочной безопасности и биосовместимости. Необходимы дополнительные уточняющие исследования для подтверждения, что те же схемы стимуляции, которые эффективны для TMС, будут эффективны и для XCS. Физиологические реакции животных и человека показывают, что DOT- и TMC-методы успешны при задействовании участков коры (мозга) площадью от 1 кв. мм до 1 кв. см с точным расчётом времени, но клиническая эквивалентность с точки зрения терапевтических результатов может быть подтверждена только после того, как имплантаты будут одобрены FDA для проведения массовых исследований на людях. Тем не менее имеются многообещающие результаты применения имплантированных эпидуральных кортикальных стимуляторов, основанных на традиционной технологии IPG и Lead, предполагающие, что электрическая стимуляция одних и тех же областей воздействия приводит и к сходным клиническим результатам.
Существуют дополнительные проблемы при создании удобного носимого DOT-передатчика. Носимые подкожные системы подзарядки разработаны и используются для существующих IPGs. Поэтому требования к аккумулятору и электронным компонентам устройств могут быть уменьшены; однако гарнитура должна быть спроектирована и протестирована настолько, чтобы обеспечить достаточный комфорт, мощность и надёжное сопряжение для частого использования дома.
Одним из преимуществ архитектуры DOT-устройств и стимуляторов XСS является способность расширять терапевтические возможности нейромодуляции при нервно-психических состояниях. К примеру, с помощью нескольких имплантатов, активируемых с точными временны́ми паттернами, уместно разрабатывать более точные (чем есть) способы модуляции состояний мозга, которые, несомненно, связаны с настроением и памятью человека. Чтобы модулировать конкретные состояния мозга с точным расчётом времени, интеграция нейронного зондирования или других сенсорных возможностей с устройствами обеспечит цикличное (непрерывное) управление мозговой активностью человека, что, как показано выше, улучшает результаты терапии. Кроме того, с новым устройством нет необходимости ездить в стационар или неподвижно сидеть в кресле. Частота и продолжительность сеансов терапии могут быть увеличены по медицинским показаниям, что прямо связано с улучшением состояния и результатами лечения.
Перспективы совершенствования устройства
В перспективах совершенствования устройства его доработка до безопасной и надёжной технологии нейромодуляции, адаптация электронного стимулятора к быту в домашнем формате применения, причём контроль и медицинское сопровождение в таком случае обеспечиваются посредством возможностей телемедицины.Об этом мы регулярно сообщаем в разделе «Новости» сайта журнала.
Это направление развития инженерной мысли перспективно, ибо домашняя терапия способна произвести революцию в лечении пациентов с депрессией. А благодаря ультрамалым размерам устройство невидимо после имплантации, но эффективно обеспечивает транскраниальную магнитную стимуляцию участков мозга и положительно влияет на облегчение состояния пациента. Таким образом, научными сотрудниками и разработчиками медицинских технологий в области микро- и наноэлектроники заявлено новое слово в системе лечения пациентов, страдающих от тяжёлых форм депрессии.
Литература
- Имплантат. Особенности и результаты исследования // URL: https://www.medrxiv.org/content/10.1101/2023.09.13.23295460v1.
- Миниатюрный имплантат для лечения депрессии // URL: https://evercare.ru/news/miniatyurnyy-implantat-dlya-lecheniya-depressi.
- Как победить осеннюю депрессию // URL: https://www.belnovosti.by/krasota-i-zdorove/psiholog-andrey-kashkarov-rasskazal-kak-pobedit-osennyuy....
- Как бороться с бессонницей при депрессии // URL: https://www.tut-news.ru/psihologiya/psiholog-andrey-kashkarov-rasskazal-kak-borotsya-s-bessonnicey-p....
- Elias G.J.B. et al. Neuromodulatory treatments for psychiatric disease: A comprehensive survey of the clinical trial landscape. Brain Stimul. Basic Transl. Clin. Res. Neuromodulation 14, 1393–1403 (2021) // URL: https://www.sciencedirect.com/science/article/pii/S1935861X21002230.
- United States Central Medical Services. LCD – Transcranial Magnetic Stimulation (TMS) in the Treatment of Adults with Major Depressive Disorder (L34998) – 2022 // URL: https://www.psychiatrist.com/jcp/depression/insurance-rtms-for-treatment-resistant-depression-mismat....
Если вам понравился материал, кликните значок — вы поможете нам узнать, каким статьям и новостям следует отдавать предпочтение. Если вы хотите обсудить материал —не стесняйтесь оставлять свои комментарии : возможно, они будут полезны другим нашим читателям!